克莱门森还原反应反应原理

反应原理:利用还原性金属在溶液中缓慢释放出的电子还原有机化合物 。如果体系中没有可供还原的有机化合物 , 那么电子的受体将只能是质子,也就是最平常的氢气制备反应 。如果有有机化合物的存在 , 例如苯乙酮,两个电子先后进入羰基的反键轨道,将双键还原,与此同时电子的进入使得分子带上负电,导致质子的进攻,这一步生成醇 。生成的醇在强酸性条件下质子化并失去一分子水,形成活性很强的碳正离子 , 而碳正离子进一步被两个电子还原,先形成不带电的自由基,然后生成带负电的碳负离子,碳负离子和体系中的质子结合,生成还原产物 。
clemmensen还原反应Clemmensen还原反应是在酸性条件下 , 用锌汞齐或锌粉还原醛基、酮基为甲基或亚甲基的反应称Clemmensen反应 。该反应使用的还原剂锌汞齐可由锌与HgCl2在稀盐酸中反应制得 。常用于芳香脂肪酮的还原,反应易于进行且收率较高 。
拓展:反应原理
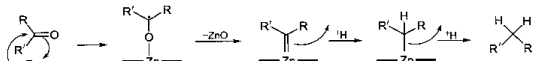
酮(或醛)与锌汞齐和盐酸共热,羰基还原为亚甲基的反应称为Clemmensen还原 。
R—C(Rˊ)═O +4(H)—→RˊCH2—R +H2O
该反应的机理尚未确定 。其中的两种观点为:
①认为还原过程开始于生成的质子化酮(或醛),然后经过自由基中间体:
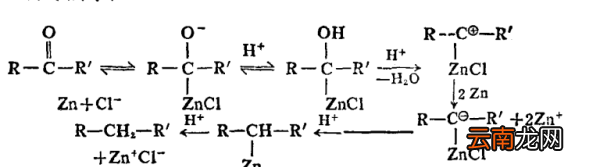
②认为是离子型机理,可能是电子从金属表面转移到羰基碳原子上:
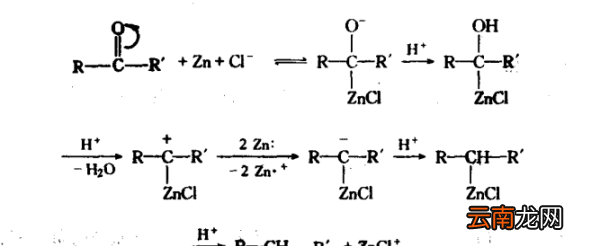
clemmensen还原法是亲核加成醛类或酮类分子中的羰基被锌汞齐和浓盐酸还原为亚甲基.
此法只适用于对酸稳定的化合物.对酸不稳定而对碱稳定的化合物可用Wolff-Kishner-黄鸣龙反应还原.
这一反应首先由英国化学家E.Clemmensen于1913年发现并用于制备烷烃、烷基芳烃和烷基酚类化合物;这个还原方法还可用于羰基酸的还原,反应的机理迄今还不十分明确 。Clemmensen还原对羰基具有很好的选择性,除 α,β-不饱和键外 , 一般对于双键无影响,而且反应操作也很简便;但是由于是在酸性介质中进行的反应 , 所以此方法不适用对酸性介质敏感的羰基化合物的还原(如呋喃醛、酮和吡咯类醛酮) 。由于是在金属表面进行的还原反应,所以还会生成一些片呐醇类的副产物 。
克莱门森还原法反应机理氢化铝锂的氢是类似于氢负离子的结构,是亲核基团 。加成碳碳双键要的是亲电试剂 , 而氢化铝锂做不到 。有机反应中羟基、醛基、羧基特别活泼都是因为O的一些性质(而胺基的活泼性是因为N的活泼性的缘故)氢化铝锂还原羧酸是因为与O形成了配合,通过一系列的排列最后形成羟基,而双键没有能与其形成配合的元素,所以不能发生反应 。
下列化学问题希望高人给予解简单说一下反应,自己写产物吧,不太好画结构式 。有不知道的找找书上的这个反应就行了
从上到下:
双键加成
第一步酯化,第二步克莱森酯缩合
形成缩酮
醚键断裂
第一步形成酰氯,第二步分子内的付氏酰基化反应 , 最后一步酮的克莱门森还原
取代羟基,注意构型
克莱森酯缩合
羟醛缩合
脱羧反应
【clemmensen还原反应,克莱门森还原反应反应原理】
推荐阅读
- 鼠标能动但点击无反应怎么办 鼠标能动但点击无反应如何处理
- 手机不小心恢复出厂设置了怎么还原 手机不小心恢复出厂设置了如何还原
- 电脑的鼠标键盘没反应怎么回事 电脑的鼠标键盘没反应是怎么回事
- 打印机打印没反应 打印机点了打印无反应的原因
- 笔记本无线鼠标没反应怎么回事 笔记本无线鼠标没反应的原因
- 笔记本无线鼠标没反应 笔记本无线鼠标没反应什么原因
- 鼠标右键没反应怎么办 鼠标右键没反应解决步骤
- 切换微信号怎么换回来 微信切换帐号怎么还原
- 浓氨水与什么反应生成一氧化氮,氨气怎么转化为一氧化氮的方程式
- 华为p9反应慢怎么办 华为p9反应慢的原因
















